 |
 |
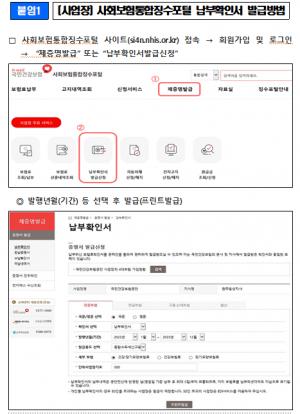
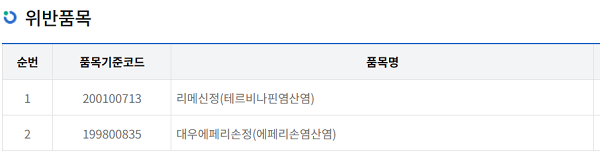
식약처는 시판 전 GMP 평가 대상 의약품 정보 미보고 혐의로 부산광역시 사하구 다대로 소재 대우제약(주)의 '리메신정(제509호)', '대우에페리손정(제391호)'에 대해 제조업무정지 1개월의 행정처분을 부과했다. 처분기간은 2023년 8월25일~9월24일까지다.
14일 식약처에 따르면 시판 전 GMP 평가 대상인 '리메신정(제509호), '대우에페리손정(제391호)'에 대해 각각 허가, 신고 변경일 이후 시판을 위해 최초로 제조한 의약품의 출하승인 예정일 30일 전에 '의약품안전나라'를 통해 해장 제품의 정보를 보고하지 않아 '의약품 등의 안전에 관한 규칙' 제48조 제14호 규정 위반, '약사법' 제76조 및 '의약품 등의 안전에 관한 규칙' 제95조 [별표8] 행정지분의 기준 II. 개별기준 제47호 규정에 의한 처분 규정을 위반한 혐의다.
이인선 기자 dailymedipharmn@gmail.com
<저작권자 © 데일리메디팜 무단전재 및 재배포금지>