 |
식약처는 올 의약품 제조.수입자 대상 위험도 평가를 기반으로 한 '품질' 중심의 현장 감시 방식으로 전면 전환키로 했다.
이는 현행 美FDA 감시기법을 참조한 정책 시행이다.
특히 GMP 6개 감시 분야 중 품질은 필수 감시하고 5개 분야는 제조소별 위험도에 따라 순환 점검키로 했다.
다만 위험도 평가 모델은 큰틀에서 유지하되 현행 3년 단위의 위험도 평가 방식을 1년으로 기간을 단축하고 평가 항목도 추가키로 했다.
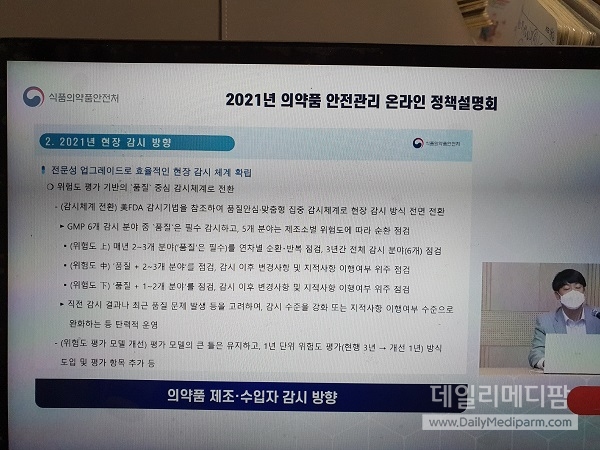
식약처는 18일 의약품 안전관리 온라인 설명회에서 '2021년 현장 감시 정책 방향'이란 발제에서 이같이 밝혔다.
'2021년 현장 감시 정책 방향'에 따르면 위험도 上인 경우 매년 2~3개 분야(품질은 필수)를 연차별로 순환, 반복 점검, 3년간 전체 6개 분야를 점검하고 위험도 中인 경우 '품질+2~3개 분야'를 점검 감시후 변경사항 및 지적사항 이행여부 위주로 점검한다. 위험도 下인 경우 '품질+1~2개 분야'를 점검, 감시후 변경사항 및 지적사항 이행여부 위주로 점검한다.
다만 직전 감시 결과나 최근 품질 문제 발생 등을 고려, 감시 수준을 강화 또는 지적 사항 이행 여부 수준으로 완화하는 등 탄력적으로 운영할 방침이다.
이를 위해 현장 경험이 풍부하고 전문성을 갖춘 인력을 현장 감시에 활용하는 체계를 구축할 예정이다. 즉 지방청 약사감시원+GMP 심시관에서 본부, 평가원, 지방청의 감시 가용 인력을 풀 가동할 예정이다.
한정렬 기자 jrh05@hanmail.net