"아스트라제네카, 일주일후엔 마지막 임상 결과까지 식약처에 제출할 것"전망
"코로나 백신 선구매후 안전성 모니터링후 접종"전략도 밝혀
학계, "아스트라제네카 코로나 백신, 심각한 부작용 없어 선구매 옳은 결정"
TF팀, 8일 브리핑 "접종 대상과 우선 순위, 추후 구체화 설명 예정"..."유통 과정 구체적인 설명 어렵다"
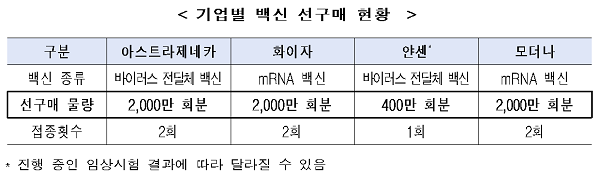 |
| ▲이날 백신 구매 TF팀이 공개한 코로나 잭신 구매 현황 자료 |
관계부처 및 민간 전문가로 구성된 백신 도입 특별전담팀(TF)은 8일 "아스트라제네카, 모더나, 화이자, 얀센 개발 코로나 백신 선구매후 안전성 모니터링 과정을 거쳐 접종하는 것이 백신 전략"이라며 "늦어도 내년말 전까지는 백신 도입이 완료될 것"이라고 밝혔다.
다만 접종 대상과 우선 순위는 추후 구체화해서 별도 설명할 예정임을 밝혔다.
백신 도입 TF팀은 이날 복지부 브리핑을 통해 이같이 코로나 백신 물량 확보 및 접종 행보를 밝혔다.
박능후 보건복지부 장관은 접종 시점을 내년 2~3월에 가능한지 여부와 관련 "백신 접종의 기존 전략은 물량은 조기 확보하더라도 접종은 신중하자는 것이다. 물론 다른 미국이나 유럽처럼 확진자수가 급증한다면 위험을 안고서라도 안전성이 확보되지 않은 상태서 접종을 강행할수도 있지만 비교적 안정적으로 코로나에 대처하고 있고 위험성이 제대로 규명되지 않은 상황에서 서둘러 접종하는 것은 필요치 않다"며 "다만 각 백신에 맞게 접종 대상을 선별해 검토하고 외국에서 2~3개월 접종후 나올수 있는 부작용들을 면밀히 모니터링후 우리 국민들에게 접종하는 것이 올바른 순서"라고 설명했다.
그렇지만 "상황이 바뀌고 국민들의 요구가 많아질 경우 보다 빠른 시일내에 접종이 가능할 것"이라면서도 "선물량 확보에 좀 더 안전성 검증과 시기를 거쳐 접종을 개시할 것"이라고 조심스런 행보를 전했다.
또 "안전성 검사는 단순 해외서 나타나는 부작용을 검증하는 것은 물론 국내 자체로도 안전성시험연구소에서 여러 검사할수 있는 장비를 활용해 독자적으로 안전성 재검토 과정을 거친 다음, 식약처 안전성 승인과 별도로 더 부가적으로 안전성 검사이후 접종 시행을 판단하고 있다"고 설명했다.
남재환 가톨릭대교수는 '아스트라제네카 백신의 임상 과정서 실수로 효능 안전성 논란임에도 정부가 선구매 계약을 체결한 이유'에 대해 "아스트라제네카의 백신은 위험하지 않다"고 밝히고 "모든 백신은 부작용이 있으며 특히 아스트라제네카의 백신 부작용은 심각하지 않은 것으로 판명이 났고 현재까지 출시된 아스트라제네카, 모더나, 화이자 백신이 이미 부작용을 공개한 바 있다. 아스트라제네카 백신이 기존 백신에 비해 심각한 부작용이 있다고 얘기할수 없는 상황이다. 따라서 선구매한 것은 전략적으로 옳은 결정"이라고 거들었다.
박 장관은 백신 도입 시기가 계약서상 특정돼 있는지와 관련 "늦어도 내년 연말까지는 백신 도입이 완료될 것"이라며 "그 이전이라도 가능한 빠른시일내에 도입될수 있게 여러 방면의 가능성을 열어두고 있다"고 말했다.
다만 아스트라제네카와 체결한 선구매 계약과 화이자, 얀센과 맺은 구매 약정서, 모더나와 맺은 공급 확약서 등 각각의 차이점과 관련 "각 개별 기업과 계약이 상이하다. 비밀 준수 의무 서약으로 그 내용에 대해 자세히 언급하기는 힘든 상황"이라고 설명했다.
양진영 식약처 차장은 '식약처에서 아스트라제네카 백신외 다른 기업의 임상 자료를 사전 검토하고 있는 것'과 관련 "아스트라제네카는지난 10월에 사전 심사를 요청했고 심사는 해당업체서 전체 자료를 완결후 제출하기 때문에 심사 기간이 늦춰질 가능성이 있어 단계별로 준비된 자료를 심사를 하게 돼 있다"며 "현재까지 비임상 자료를 심사 중에 있으며 아스트라제네카외에 다른 기업에서는 사전 심사를 요청해 온 바 없다"고 밝혔다.
박 장관은 이어 "최근 정부와 아사트라제네카간 협의과정에서 아스트라제네카의 백신 경우 앞으로 일주일후에 마지막 임상 결과까지 식약처에 제출할 것으로 전망된다"고 말했다.
다만 국내 냉장.냉동업체가 소수인데 어떤 해결책을 갖고 있는지 여부에 대해 "접종 대상과 우선 순위는 추후 구체화해서 별도 설명할 예정이며 당장 답변하긴 곤란하다"며 백신 도입후 유통과정 또한 구체적인 설명은 어렵다고 했다.
한편 백신 도입 TF팀은 이날 코박스 퍼실러티(COVAX Facility)를 통해 약 1000만명분, 글로벌 백신 기업에서 약 3400만명분(최대 6400만 회분) 등 최대 4400만명분의 해외개발 백신을 선구매한다고 밝혔다.
최대 6400만 회분은 아스트라제네카 2000만 회분, 화이자 2000만 회분 및 얀센 400만 회분, 모더나 2000만 회분이다.
정부는 백신 선급금 지급 및 백신 구매를 위해 2020년 예산 중 이·전용분 1723억원, 4차 추경 1839억원 및 2021년도 목적예비비 9천억원 등 약 1조3천억원의 예산을 확보했다.
한정렬 기자 jrh05@hanmail.net