(주)삼양바이오팜 항암제 '제넥솔피엠주' 등 파클리탁셀 7품목이 시판후 조사에서 '종양 용해 증후군'이 추가 보고됐다.
 |
식약처는 '파클리탁셀'함유제제의 유럽 EMA 및 美FDA 안전성 정보와 관련 국내·외 허가 현황, 제출의견 등을 종합 검토한 결과에 따라 허가사항 변경지시 할 계획이며 오는 26일까지 사전예고 한다고 밝혔다.
허가사항 변경안에 따르면 '삼양바이오팜파클리탁셀주' 등 4품목은 시판후 조사에서 이 약 투약후에 피부의 광범위 부종, 비후화, 경화외에 종양 용해 증후군이 보고됐다.
또 제넥솔피엠주, 제넥솔피엠주100mg, 리포락셀액 등 3품목은 시판 후 조사에서 파클리탁셀 성분 제제를 투여받은 환자에게서 종양용해증후군이 보고됐다.
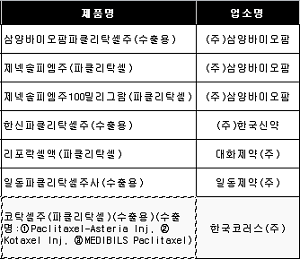
해당 제품은 (주)삼양바이오팜 '삼양바이오팜파클리탁셀주(수출용)', '제넥솔피엠주', '제넥솔피엠주100mg', (주)한국신약 '한신파클리탁셀주(수출용)', 대화제약(주) '리포락셀액', 일동제약(주) '일동파클리탁셀주사(수출용)', 한국코러스(주) '코탁셀주(파클리탁셀)(수출용)' 등 7품목이다.
이인선 기자 eipodo@naver.com
<저작권자 © 데일리메디팜 무단전재 및 재배포금지>






