유럽 의약품청(EMA)은 '히드록시우레아' 성분제제에 대한 이상반응으로 '간질성폐질병', '피부암' 등을 보고했다
식약처는 이같은 안전성 정보에 대한 검토결과에 따라 해당 품목에 대해 허가 변경이 필요하다고 판단, 허가사항 변경안을 마련했다며 해당제약사는 검토의견이 있는 경우 해당 사유 및 근거자료를 26일까지 제출해 줄것을 13일 주문했다.
사용상의주의사항에 따르면 확산성 폐침윤, 발열, 호흡곤란과 같은 급성 폐반응의 발생과 이 약과의 연관성이 드물게 보고된 것과 '폐섬유증'외에 '간질성폐질병'이 드물게 보고됐다.
또 피부암이 장기간 동 성분을 투여받은 환자에게서 보고됐으며 환자는 태양 노출로부터 피부를 보호해야 한다고 주의시켜야 한다.
또한 환자는 동 성분 치료중과 치료 중단 후 피부의 자가 진단을 이행해야 하며 정기적으로 후속 방문해 2차 종양(malignancies)발생 가능성에 대한 검진해야 한다.
아울러 골수증식질환 환자에서 폐섬유증, 폐침윤, 폐렴 및 폐포/알레르기성 폐포염을 포함한 간질성 폐질병이 보고되었으며, 치명적인 결과와 관련이 있을 수 있다.
발열, 기침, 호흡 곤란 증세를 보이는 환자는 면밀히 모니터링하고 조사 및 치료해야 하며 이 약의 신속한 중단과 코르티코스테로이드 치료는 폐 반응의 해소와 관련이 있는 것으로 보인다는 일반 주의사항도 신설됐다.
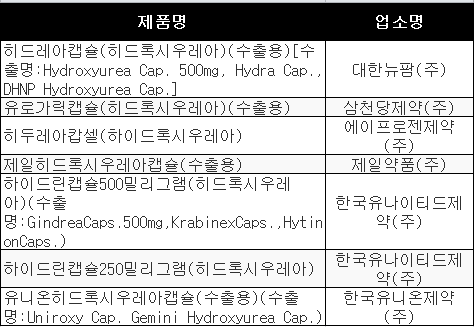
해당 품목은 한국유나이티드제약(주) '하이드린캡슐500mg', '하이드린캡슐250mg', 한국유니온제약(주) '유니온히드록시우레아캡슐', 대한뉴팜(주) '히드레아캡슐', 삼천당제약(주) '유로가릭캡슐', 에이프로젠제약(주) '히두레아캅셀', 제일약품(주) '제일히드록시우레아캡슐(수출용)' 등 7품목이다.
 |
한정렬 기자 jrh05@hanmail.net